II Die Einteilung der Stoffe
2.1 Wie können wir die Stoffe einteilen?
So können wir die Stoffe einteilen:
a) In Feststoffe, Flüssigkeiten und Gase
b) In Metalle und Nichtmetalle
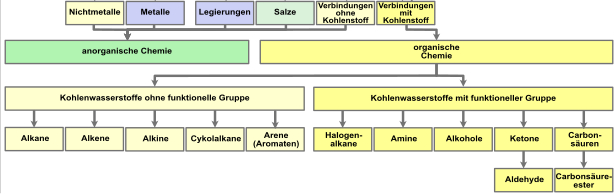
c) In organische und anorganische Stoffe
III Was sind organische und anorganische Stoffe?
3.1 Organische Stoffe



Organische Chemie und anorganische Chemie sind zwei Hauptzweige der Chemie. Sie befassen sich mit unterschiedlichen Arten chemischer Verbindungen. – Grob gesagt handelt es sich bei den organischen Stoffen um Stoffe aus der belebten Natur. Die Stoffe aus der anorganischen Chemie kommen aus der unbelebten Natur.
Organische Chemie konzentriert sich auf Kohlenstoffverbindungen, insbesondere solche, die Kohlenstoff-Wasserstoff-Bindungen enthalten. – Organische Moleküle bestehen also meist aus Kohlenstoff-, Wasserstoff-, Sauerstoff- und Stickstoffatomen.
Beispiele für organische, also kohlenstoffhaltige Stoffe sind Erdöl, Erdgas, Benzin, Diesel, Kerosin, Kohle, Zucker, Mehl oder Holz.
Woran erkennst du organische Stoffe?
Organische Stoffe erkennst du an
- Verkohlen beim Erhitzen
- Verbrennen mit rußig-schwarzer Flamme
Experiment 1: Wird das Glas schwarz?
Experiment 1:
Halte ein Reagenzglas über die Flamme eines Teelichtes und drehe das Reagenzglas mehrere Male.
Was beobachtest du nach kurzer Zeit?
Beobachtung: Das Glas wird schwarz. Auf dem Glas lagert sich Ruß ab. Dieser besteht aus Kohlenstoff, welcher aus dem Wachs und dem Docht entstand. Wachs und Docht sind also organische Verbindungen.
3.2 Anorganische Stoffe



Experiment 2:
Welche Stoffe sind organisch oder anorganisch?
Material:
3 Reagenzgläser, Reagenzglashalter (Holzklammer), Reagenzglasgestell, Salz, Mehl, Holzspan und Brenner.
Durchführung:
Gib in das 1. Reagenzglas etwas Salz, in das 2. Reagenzglas etwas Mehl und in das dritte Reagenzglas den Holzspan. – Erhitze nun nach der Reihe die Reagenzgläser samt Inhalt. – Was kannst du beobachten?
Beobachtung und Erkenntnis:
Salz verändert seine Farbe nicht. – Es ist daher anorganisch.
Mehlr und Holzspan werden schwarz. Sie enthalten also Kohlenstoff und sind organisch.
Die anorganische Chemie (Anorganik) untersucht alle anderen Elemente und ihre Verbindungen, also jene, die typischerweise keine Kohlenstoff-Wasserstoff-Bindungen aufweisen
Beispiele für anorganische Stoffe oder Moleküle sind Schwefel, Kupfersulfat, Kochsalz, Wasser, Glas, Silizium, oder Phosphor.
Organische Chemie
Anorganische Chemie
- Fokus: Kohlenstoffverbindungen, insbesondere Kohlenwasserstoffe und deren Derivate (davon abgeleiteten Verbindungen).
- Merkmale: Enthält oft komplexe Moleküle mit kovalenten Bindungen/Atombindungen (bei denen sich zwei Atome ein oder mehrere gemeinsame Elektronenpaare teilen) zwischen Kohlenstoff und anderen Elementen wie Wasserstoff, Sauerstoff, Stickstoff, usw.
- Beispiele: Kohlenhydrate, Proteine, Fette, Kunststoffe, Medikamente
- Fokus: Alle anderen Elemente des Periodensystems und ihre Verbindungen (außer den oben genannten organischen Kohlenstoffverbindungen).
- Merkmale: Kann ionische (eine chemische Bindung, die durch die elektrostatische Anziehung zwischen entgegengesetzt geladenen Ionen entsteht) oder kovalente Bindungen (Atombindung bzw. Elektronenpaarbindung) beinhalten, oft einfachere Moleküle als in der organischen Chemie.
- Beispiele: Metalle, Salze, Säuren, Basen, Wasser, Mineralien
Überschneidungen
Die Unterscheidung ist nicht immer klar, da es Ausnahmen gibt. Zum Beispiel gelten einige Kohlenstoffverbindungen, wie Kohlenstoffdioxid, Kohlenmonoxid und Carbonate, als anorganisch.
Geschichtlich
Früher wurde die organische Chemie mit „Lebenskraft“ verbunden, da man dachte, dass organische Stoffe nur von Lebewesen hergestellt werden können. Durch die Synthese von Harnstoff durch Friedrich Wöhler im Jahr 1828 wurde dies widerlegt.